Phase III Studie zur Therapie des klarzelligen Nierenzellkarzinoms
ARISER STUDIE
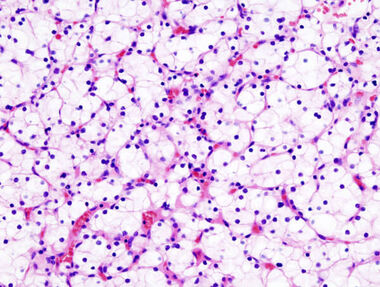
Randomisierte Studie zur adjuvanten Therapie des klarzelligen Nierenzellkarzinoms mit dem Antikörper cG250 (ARISER- Studie) richtet sich an alle Patienten mit einem klarzelligen Nierenzellkarzinom, bei denen der Tumor operativ entfernt wurde und bei denen keine Fernabsiedelung (Metastasierung) des Tumors vorliegt. Aufgrund des vorliegenden Risikoprofils, welches sich während der Operation und in der nachfolgenden Feingewebsuntersuchung zeigt, besteht jedoch möglicherweise ein erhöhtes Risiko für ein Rezidiv (Neuauftreten) des Nierenzellkarzinoms. Ziel dieser randomisierten verblindeten Phase III Studie ist die Beurteilung der Wirksamkeit einer adjuvanten Therapie mit dem Antikörper cG250 (Rencarex®) im Vergleich zum Placebo, um ein mögliches Rezidiv des Tumors zu vermeiden.
Allgemeines: Nach operativer Therapie eines klarzelligen Nierenzellkarzinoms, wenn keine weitere Metastasierung des Tumors vorliegt, erfolgen in der Regel regelmäßige Krebsnachsorgeuntersuchungen zusammen mit bildgebenden Untersuchungen. So soll ein mögliches Wiederauftreten des Tumors rechtzeitig erkannt und behandelt werden. Zur Weiterentwicklung der derzeit bestehenden Therapiemöglichkeiten sind Ärzte in Zusammenarbeit mit der pharmazeutischen Industrie bemüht, die bestehenden Therapieformen zu verbessern. Die Teilnahme an solchen klinischen Studien ist stets freiwillig. Die Durchführung dieser Studie erfolgt nach den bestehenden Prinzipien des Weltärztebundes (Deklaration von Helsinki), dem deutschen Arzneimittelgesetz, den Regularien der amerikanischen Gesundheitsbehörde („Food and Drug Administration“; FDA) und den internationalen Richtlinien der „good clinical practice“ (GCP).
Ziel der Studie: Nach erfolgter Nephrektomie (Nierenentfernung), wenn keine weitere Metastasierung im Körper vorliegt, besteht kein Anhaltspunkt für sichtbares Tumorgewebe beim Patienten. Die Tumorgröße, die Ausbreitung des Tumors, ein eventueller Befall von Lymphknoten geben dem behandelnden Arzt jedoch Hinweise für das Risiko eines möglichen Wiederauftretens des Tumors. Nach der durchgeführten Entfernung aller bekannten Tumorlokalisationen wird in diesem Stadium normalerweise keine weitere Therapie eingeleitet. Es erfolgt die regelmäßige Tumornachsorge. Rahmen der klinischen Prüfung mit einem nicht-zugelassenen Medikament, dem Antikörper cG250, soll bei Patienten mit einem erhöhten Risiko für ein Tumorrezidiv (s. Einschlusskriterien) eine Verminderung oder Vermeidung des Wiederauftretens des Tumors erreicht werden. Die Behandlung mit dem Antikörper cG250 erfolgt im Rahmen einer Phase III Studie (sog. ARISER-Studie: Adjuvant Rencarex® Immunotherapy Phase III trial to Study Efficacy in non-metastatic Renal cell carcinoma).
Wann liegt ein erhöhtes Risikoprofil vor? Wann kann ich an der Studie teilnehmen? Ob bei Ihnen ein erhöhtes Risikoprofil für ein Wiederauftreten des Nierenzellkarzinoms vorliegt und Sie an dieser Studie teilnehmen können, klären wir gerne in einem persönlichen Gespräch in unserer urologischen Ambulanz.
In die ARISER-Studie könne alle Patienten mit einem klarzelligen Nierenzellkarzinom nach erfolgter Nephrektomie eingeschlossen werden. Bei der Operation sollte sowohl mikroskopisch (feingeweblich) als auch makroskopisch (mit dem „bloßen Auge“) Tumorfreiheit bestehen. Der Operationszeitpunkt darf dabei nicht länger als 8 Wochen zurückliegen, um mit der Studie beginnen zu können.
Nach der Operation erfolgt durch den Pathologen die Einteilung des Tumors in eine feste Klassifikation, die sog. TNM Klassifikation. Eine Teilnahme an der Studie ist möglich bei folgenden Tumorstadien (TNM Klassifikation, 6. Auflage, UICC 2002):
- Histologisch nachgewiesen: >=pT3bN0/NxM0 oder pT3cN0/NxM0 oder pT4N0/NxM0
- Histologisch nachgewiesen: jedes T-Stadium mit N+ und M0
- Histologischer Primärtumor: pT1bN0/NxM0 oder pT2N0/NxM0 und mikroskopische Gefäßinvasion und mindestens Grad III oder pT3aN0/Nx/M0
Wirkung des Medikamentes: Der Antikörper cG250 (Rencarex®) erkennt und bindet sehr spezifisch an Nierenkrebszellen. Mit der Anheftung des Antikörpers an die Krebszellen erfolgt eine „Markierung“, und der körpereigene Mechanismus der Immunabwehr wird aktiviert und führt nachfolgend zur Zerstörung dieser Krebszellen. Normalgewebe ist von diesem Vorgang nicht betroffen. In mehreren bereits mit diesem Antikörper durchgeführten klinischen Studien konnte eine gegen den Tumor gerichtete Wirkung beobachtet werden. Diese Patienten wiesen jedoch -im Gegensatz zur jetzigen klinischen Prüfung- alle ein fortgeschrittenes Nierenzellkarzinom mit Fernabsiedlungen in anderen Organen auf.
Mögliche Vorteile durch die Studienteilnahme: Bei dem verwendeten Medikament Rencarex® handelt es sich um ein neues Präparat, so dass ein günstiges Ansprechen auf die Behandlung nicht vorhergesagt und garantiert werden kann. Derzeit ist auch eine medikamentöse Therapie von Patienten nach einer Operation eines Nierenzellkarzinoms ohne sichtbare Tumorreste nicht üblich. Die bislang vorliegenden Daten zur Wirksamkeit des Antikörpers cG250 (Rencarex®) wurden ausschließlich an Patienten mit einem fortgeschrittenen Nierenzellkarzinom erhoben. Diese Patienten hatten bereits vor Beginn der Behandlung vorliegende Fernmetastasen. Die Ergebnisse dieser Studien zeigten eine sehr gute Verträglichkeit und wiesen auf eine Tumorstabilisierung und Anti-Tumorwirkung hin.
Die ARISER-Studie ist die erste Anwendung des Antikörpers bei Patienten ohne nachweisbare Metastasen oder Reste des Ursprungstumors. Hierbei soll die Annahme geprüft werden, dass die Gabe des Antikörpers das Wiederauftreten (Rezidiv) des Nierenzellkarzinoms verzögern oder hindern kann. Die Teilnahme an dieser klinischen Prüfung ist freiwillig.
Durchführung der Studie: Sollten Sie Interesse an dieser Studie haben und an dieser Studie teilnehmen können, so erfolgt innerhalb der ersten 8 Wochen nach der Nierenentfernung der Studienbeginn. Hierbei wird nach erfolgter Randomisierung (Zufalls mäßige Einteilung in eine Therapiegruppe) das Medikament Rencarex® oder Placebo verabreicht. Die Medikamentengabe erfolgt unter ärztlicher Kontrolle einmal wöchentlich über einen Behandlungszeitraum von 24 Wochen. Nach der durchgeführten Therapiephase schließt sich eine engmaschige Nachsorgekontrolle an.
Für weiterführende Informationen zur Studie und einer möglichen Teilnahme können Sie sich jederzeit an unserer Ärzte der urologischen Ambulanz oder direkt an Hr. PD. Dr. med. A. Haferkamp.