DANBUE
Eine Phase III, randomisierte, unverblindete, multizenterische, globale Studie zur Bewertung einer Erstlinientherapie mit Durvalumab als Einzelwirkstoff und Durvalumab in Kombination mit Tremelimumab gegenüber der Standard-Chemotherapie bei Patienten mit einem inoperablen Grad 4 Urothelkarzinom
Beschreibung:
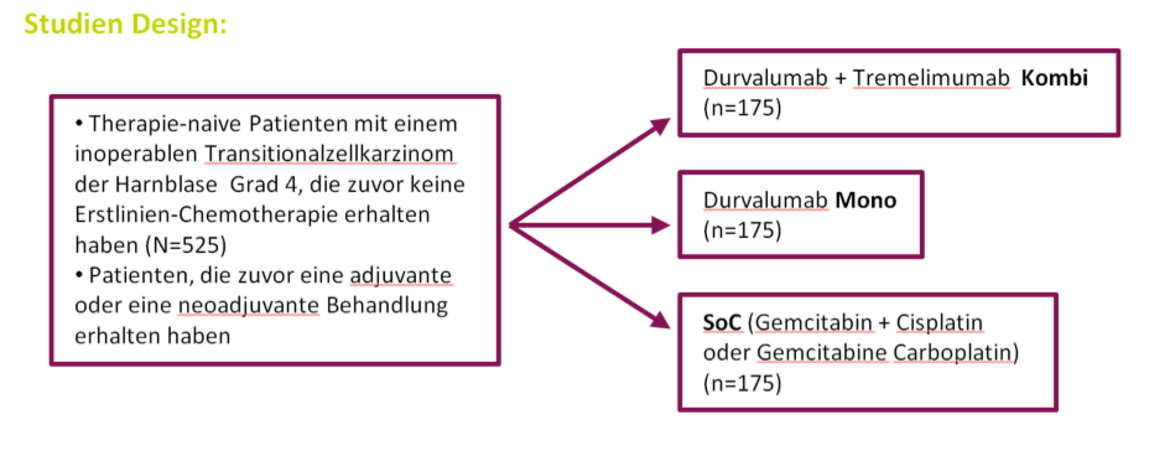
Es handelt sich um eine randomisierte, unverblindete, kontrollierte, globale Multizenterstudie der Phase III zur Feststellung der Wirksamkeit und Sicherheit einer Durvalumab Monotherapie, und Durvalumab in Kombination mit Tremelimumab im Vergleich zur Standardtherapie (Cisplatin + Gemcitabin oder Carboplatin + Gemcitabin) als Erstlinientherapie bei Therapie-naiven Patienten mit einem histologisch oder zytologisch dokumentierten, inoperablen Transitionalzellkarzinom Grad 4 (Transitionalzellkarzinom und gemischte Transitional-/Nicht-Transitionalzellhistologien) des Urothels.
Hintergrund:
Tumorzellen können die Immunabwehr verhindern, indem sie bestimmte Botenstoffe zur Hemmung des Immunsystems produzieren. Hierzu zählen unter anderem der PD-Ligand (PD-L1) aber auch das Oberflächenprotein CTLA-4. Über diese Wege die Funktion von T-Zellen herunterreguliert und damit die Krebsbekämpfung behindert. Durvalumab (MEDI4736) als Antikörper bindet gezielt an den PD-L1 Rezeptor der Tumorzelle. Die immunmodulatorische Substanz Tremelimumab (CTLA-4-Antikörper) bindet an das Oberflächenprotein CTLA-4. Die Tumorzelle kann nach Bindung einer dieser Substanzen nicht mehr eine Hemmung der T-Zelle auslösen. Die T-Zellen können nun ihre Immunreaktion auf die Tumorzellen ausüben und somit die Krebszelle besiegen.
Endpunkte:
Primärer EP:
- Progressionsfreies Überleben (PFS)
Sekundäre EPs:
- Progressionsfreies Überleben bei PD-L1(-) Patienten
- Gesamtüberleben (OS)
- Objektive Ansprechrate (ORR)
- Functional Assessment of Cancer Therapy Bladder Cancer (FACT BL)
- Medikamenten Antikörper (ADA)
- Pharmakokinetik
- Sicherheit und Verträglichkeit
Wichtige Einschlusskriterien:
- Alter 18+
- Patienten mit histologisch oder zytologisch gesichertem, inoperablen Transitionalzellkarzinom der Harnblase Grad 4, die nicht zuvor mit einer Erstlinien-Chemotherapie behandelt worden sind
- Patienten, die sich für eine Cisplatin-basierte Chemotherapie eignen /nicht eignen
- Eine fehlende Eignung für eine Behandlung mit Cisplatin liegt vor, wenn eines der folgenden Kriterien erfüllt ist:
- Kreatinin-Clearance (berechnet od. gemessen) <60mL/min
- Audiometrischer Hörverlust ≥ CTCAE Grad 2
- CTCAE Grad 2 Periphere Neuropathie
- NYHA Grad III Herzinsuffizienz
- Eine fehlende Eignung für eine Behandlung mit Cisplatin liegt vor, wenn eines der folgenden Kriterien erfüllt ist:
- Vor Randomisierung bekannter Tumor PD-L1 Status (Immunohistochemier Nachweis durch ein Referenzlabor)
Wichtige Ausschlusskriterien:
- Vorherige Exposition gegenüber einer immun-vermittelten Therapie, einschließlich jedoch nicht beschränkt auf:
- Andere anti-zytotoxische T-Lymphozyten-assoziierte Antigen-4 (CTLA-4) Antikörper
- Andere Anti-PD-1, Anti-PD-L1 oder Anti-PD-L2 Antikörper, einschließlich therapeutischer Antikrebsimpfungen
- Vorherige Organtransplantation, die eine Behandlung mit Immunsuppressiva erforderlich macht
- Aktive oder zuvor dokumentierte Autoimmunerkrankungen oder entzündliche Erkrankungen innerhalb 3 Jahre vor Beginn der Behandlung
- Hirnmetastasen oder Rückenmarkskompression (Bei Patienten mit Verdacht auf Hirnmetastasen im Screening sollte ein cCT/cMRT vor Eintritt in die Studie durchgeführt werden)
- Aktive Infektion, u.a. Hepatitis B, Hepatitis C oder HIV
- Aktuelle oder vorausgehende Anwendung von Immunsuppressiva binnen 14 Tagen vor der ersten Dosis Prüfpräparates
- Patienten, die in den 30 Tagen vor der ersten Dosis des Prüfpräparates einen abgeschwächten Lebendimpfstoff erhalten haben
-- Follow Up --