Pathophysiologie des Aortenaneurysmas
Erweiterungen der Bauchschlagader (abdominelle Aortenaneurysmen, AAA) treten vorwiegend bei Männern im Alter von über 65 Jahren auf. Die Ruptur eines solchen AAA ist akut lebensbedrohlich, seine Pathogenese jedoch bisher kaum verstanden. Histopathologische Kennzeichen des AAA sind Verdickung und Fibrosierung der Aortenwand, Verlust glatter Muskelzellen und Degeneration der stabilisierenden Proteinfasern. Außerdem werden Entzündungs- und Immunreaktionen in der Gefäßwand des AAA beobachtet. Ziel unserer Untersuchungen ist es, die molekularen Entzündungs- und Heilungsprozesse in der Aorta besser zu verstehen, und somit die Voraussetzung für neue Therapieansätze des AAA zu schaffen.
(1) Pathophysiologische Mechanismen des zytoplasmatischen DNA-Sensors AIM2 in der Entstehung und Progression des abdominellen Aortenaneurysmas (AAA)
| Projektleiter: | Prof. Dr. rer. nat. Susanne Dihlmann, Dr. med. Markus Wortmann |
| Förderung: | Deutsche Forschungsgemeinschaft, DFG (2016-2020) |
| Wiss. Mitarbeiter: | Dr. rer. nat. Muhammad Arshad (seit 2019) |
| Doktoranden: | MSc. Ekaterina Skorubskaja (2017-2018) |
| Laborassistenz: | Anja Spieler (Biologielaborantin) |
Das Absent-in-Melanoma-2 (AIM2)-Protein ist Bestandteil der angeborenen Immunantwort. In Entzündungs- und Immunzellen erkennt es fremde DNA, die von Viren oder Bakterien stammt und löst zusammen mit anderen Proteinen eine Kaskade von Signalen aus, die der Infektionsabwehr dienen. Neuere Erkenntnisse zeigen, dass AIM2 auch in gesunden, nicht-Immunzellen produziert wird, wenn fremde DNA, z.B. von absterbenden Nachbarzellen erkannt wird. Auch hier wird anschließend eine Kaskade von Signalen ausgelöst, die Entzündungszellen anlockt und das betroffene Gewebe verändert. In wieweit hier AIM2 wichtig für den Heilungsprozess ist, oder ob es zur Zerstörung des Gewebes durch chronische Inflammation beiträgt, ist Gegenstand unserer Untersuchungen.
Um die Funktion von AIM2 in der Entstehung des AAA in vivo untersuchen zu können, setzen wir Mausmodelle ein, die aufgrund gezielter genetischer Veränderungen unterschiedlich empfänglich für die Angiotensin II-induzierte Entstehung von Aortenaneurysmen sind (ApoE Knockout und Aim2 Knockout). Erste Ergebnisse aus diesen Experimenten deuten darauf hin, dass AIM2 eine protektive Wirkung im Verlauf des AAA hat, indem es die Differenzierung glatter Gefäßmuskelzellen beeinflusst.
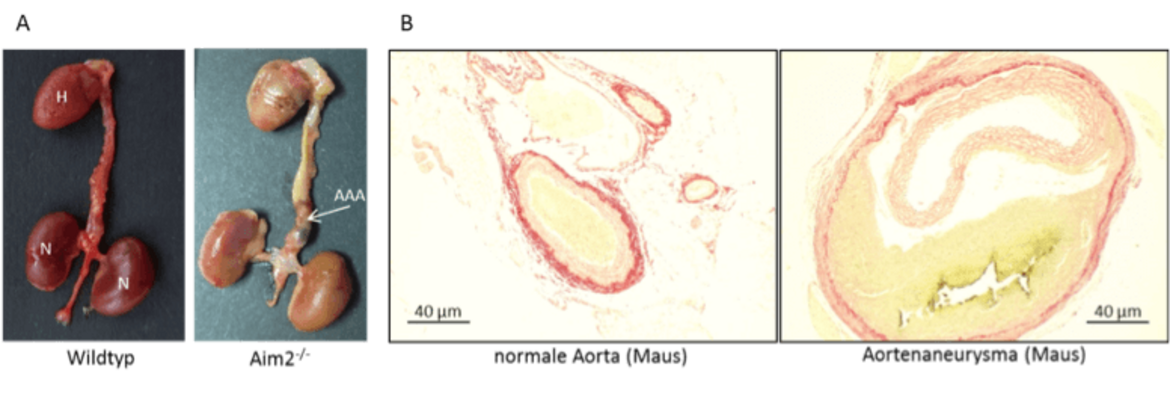
Ergänzend zu den in vivo-Untersuchungen am Mausmodell führen wir Zellkultur-Studien zur Funktion von AIM2 an Gefäßmuskelzellen der Aorta (AoSMC) durch. Hierbei kommen sowohl Zellen aus der Aorta der Mausmodelle als auch Zellen aus Patientengewebe zum Einsatz.
(2) Oxidativer Stress in vaskulären Zellen in der Entstehung Abdomineller Aortenaneurysmen
| Projektleiter | Dr. med. Markus Wortmann |
| Förderung | Stiftung Chirurgie Heidelberg (2019) Stiftung Chirurgie Heidelberg (2016) Majic-Schlez-Stiftung (bis 2018) |
| Doktoranden | Adrian Abele (2016 bis 2019) |
| Laborassistenz | Anja Spieler (Biologielaborantin) |
Als oxidativer Stress wird ein Stoffwechselzustand bezeichnet, bei der intrazellulär ein Überschuss an reaktiven Sauerstoffverbindungen (ROS –reactive oxygen species) vorliegt. Diese reaktiven Sauerstoffverbindungen entstehen im Rahmen von Stoffwechselvorgängen in Mitochondrien und können zu Schäden an der DNA, Lipiden und Proteinen der betroffenen Zellen führen. Als Reaktion werden Entzündungsmechanismen ausgelöst, die weitere Schädigungen, wie vaskuläre Dysfunktion, verursachen. Auch an der Entstehung und Progression des Aortenaneurysmas ist oxidativer Stress beteiligt, ausgelöst u.a. durch Tabakgifte oder Bluthochdruck. Die molekularen Mechanismen dieser Schädigung sind bisher jedoch weitgehend unbekannt.
Mit Hilfe von Mausmodellen, untersuchen wir, wie sich oxidativer Stress auf Signalmechanismen in glatten Gefäßmuskelzellen (VSMC) und Endothelzellen (EC) auswirkt, und welche pharmakologischen Wirkstoffe diesem oxidativer Stress entgegenwirken, um so die Entstehung und/das Wachstum von Aortenaneurysmen zu verlangsamen. Zum einen setzten wir Mausmodelle ein, die sich bezüglich eines mitochondrialen Proteins der Atmungskette unterscheiden, und daher unterschiedlich empfindlich gegenüber der Angiotensin II-induzierten Entstehung von Aortenaneurysmen sind. Zum anderen werden Mausmodelle mit einem Defekt im Lipidstoffwechsel (ApoE Knockout) untersucht.
(3) Rupturrisiko bei abdomineller Aortenaneurysmen
| Projektleiter: | Dr. med. Philipp Erhart |
| Förderung: | B. Braun-Stiftung Stiftung Chirurgie Heidelberg Aortenpreis der Deutschen Gesellschaft für Gefäßchirurgie |
| Doktoranden: | Sandra Schiele (2014-2019) Amelie Luka Behrens (seit 2017) |
| Laborassistenz: | Anja Spieler (Biologielaborantin) |
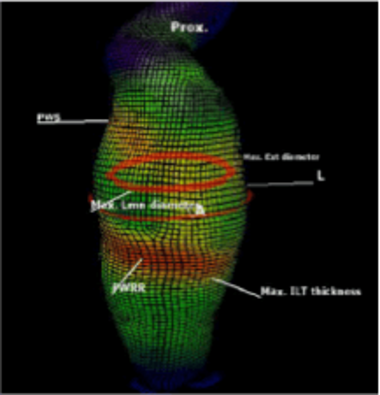
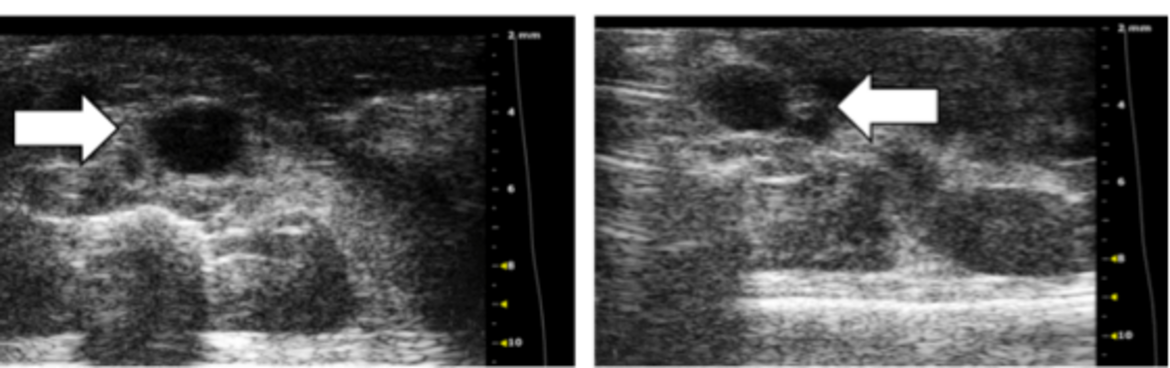
Die Ruptur eines Bauchaortenaneurysmas ist ein lebensbedrohlicher Zustand. Die rechtzeitige Diagnose und chirurgische Therapie sind essentiell. Trotz entscheidender Fortschritte in der bildgebenden Diagnostik abdomineller Aortenaneurysmata ist die genaue Vorhersage des Rupturrisikos weiterhin unklar. In der klinischen Praxis werden der Durchmesser und die Expansionsrate des Aneurysmas als entscheidende Kriterien zur operativen Versorgung herangezogen.
Ziel des Forschungsvorhabens ist es anhand eines computertomographiebasierten Finite Elemente Models und Gewebeuntersuchungen aus Gefäßwandproben weitere Erkenntnisse zur Entstehung und Risikovorhersage von Aortenaneurysmen zu gewinnen. Hierfür kommen histologische, molekularbiologische und genetische Verfahren zur Anwendung die mit Daten aus biomechanischen Berechnungen des Aneurysmas kombiniert werden. Eine patientenspezifischere Rupturrisikovorhersage soll damit in Aussicht gestellt werden.
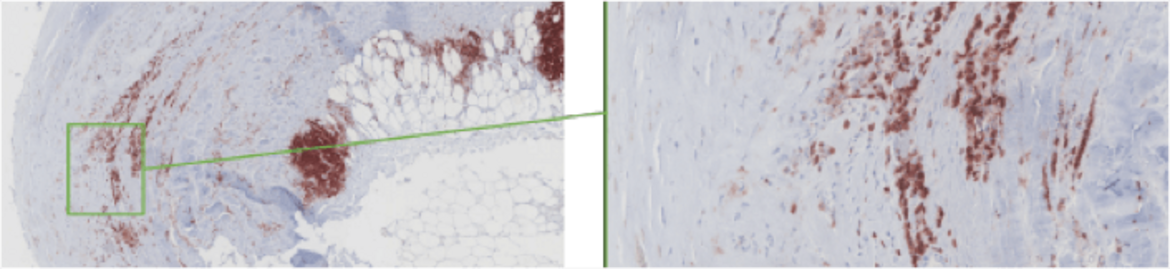
(4) Identifikation von genetischen Risikofaktoren bei Aortendissektionen
| Projektleiter: | Dr. med. Philipp Erhart |
| Förderung: | B. Braun-Stiftung Stiftung Chirurgie Heidelberg Deutsche Gesellschaft für Gefäßchirurgie (Forschungsstipendium) |
| Kooperationen: | PD Dr. rer. nat. Caspar Grond-Ginsbach, Neurologische Klinik DKFZ Heidelberg Helmholtz Zentrum München |
Die akute Aortendissektion Typ B ist charakterisiert durch einen Einriss der inneren Gefäßschicht mit resultierender Einblutung in die Brustschlagaderwand. Therapeutisch wird nach klinischen und bildmorphologischen Kriterien ein konservatives oder operatives Verfahren gewählt um die Progression und Mortalität der Erkrankung zu vermindern. Die Entstehung ist multifaktoriell und weitestgehend ungeklärt. Neben Trauma und den typischen Risikofaktoren für Herz-Kreislauferkrankungen wie Bluthochdruck und Rauchen kommen auch genetische Ursachen in Betracht.
Hierfür sollen an unserem Aortenzentrum bei Patienten mit Aortendissektionen Blutproben für genetische Analysen entnommen und ausgewertet werden. Hautgewebeproben für eine elektronenmikroskopische Untersuchung sollen die Befunde aus der Genetik ergänzen um Bindegewebsdefekte zu identifizieren. Das Ziel der Studie ist neue genetische Risikovarianten bei Patienten mit nichttraumatischen Aortendissektionen zu identifizieren und deren Bedeutung für den klinischen Krankheitsverlauf zu untersuchen. Eine fachgenetische Beratung soll für junge Patienten und deren Familienangehörige angeboten werden.
(5) Epidemiologische und histopathologische Untersuchung multipler Aneurysmen
| Projektleiter: | PD Dr. med. Maani Hakimi |
| Doktoranden: | Daniel Körfer (seit 2016) |
| Laborassistenz: | Anja Spieler (Biologielaborantin) |
Klinische Beobachtungen zeigen deutliche Unterschiede im Krankheitsbild „arterielles Aneurysma“ bezüglich Elongation, Thrombus, Kalzifikation oder Anzahl der auftretenden Aneurysmen. Die chirurgische Versorgung arterieller Aneurysmen erfolgt derzeit mit einheitlichen Verfahren, ohne Berücksichtigung der biologischen Diversität oder der Ätiologie in der betroffenen Gefäßregion. Möglicherweise haben unterschiedliche Entstehungsmechanismen jedoch einen Einfluss auf den Verlauf der Erkrankung, so dass die Patienten von einer individuell angepassten Methodenwahl zur Versorgung profitieren würden.
Um die Ursachen der unterschiedlichen Aneurysmabeschaffenheit besser verstehen zu können, setzen wir epidemiologische Analysen anhand von Patientendaten vergangener Jahre ein. Bisher erfolgte eine retrospektive Analyse epidemiologischer Daten von Patienten, die im Zeitraum von 2006 bis 2016 an unserer Klinik behandelt worden sind. Hierbei wurden Alter, Geschlecht und histologisch sichtbare inflammatorische Parameter der Patienten zweier Gruppen (Patienten mit singulärem Aneurysma versus Patienten mit drei oder mehr Aneurysmen im Untersuchungszeitraum) verglichen. Insgesamt konnten so Daten von über 2000 Patienten mit arteriellen Aneurysmen untersucht werden. Bei Patienten mit multiplen Aneurysmen zeigte das Verteilungsmuster eine starke Ausprägung im Bereich der Becken- und Poplitealarterien. Patienten dieser Gruppe waren außerdem signifikant jünger bei Erstdiagnose eines Aneurysmas und signifikant seltener weiblichen Geschlechts als Patienten mit singulärem AAA. Die histopathologischen Analysen ergaben des weiteren Unterschiede in der Degradation von Extrazellulärmatrix sowie inflammatorischen Prozessen in der Gefäßwand. Insgesamt bestärken die Ergebnisse die Vermutung, dass sich die Ursachen und Verläufe singulärer bzw. multipler Aneurysmen epidemiologisch und biologisch unterscheiden.
In weiterführenden Studien wollen wir die hierfür zugrunde liegenden genetischen Ursachen (Polymorphismen, Nachweis von Mutationen in Bindegewebsgenen, etc.) genauer untersuchen.