Forschungsgruppe Neuro-Radioonkologie
Die Arbeitsgruppe Neuro-Radioonkologie befasst sich mit der Erforschung strahlentherapeutischer Verfahren und Therapieansätze bei der Behandlung von primären und sekundären Tumoren im Bereich des Nervensystems. Dabei handelt es sich um eine Vielzahl an Tumorentitäten:
Hierunter fallen nicht nur primäre Hirntumoren wie z.B. die Gliome, das Glioblastom u.v.m., sondern auch gutartige und bösartige Tumoren der Hirnhäute (Meningeome) und Hirnnerven/Spinalnerven (Neurinome/Schwannome), aber auch sekundäre Hirntumoren wie Hirnmetastasen, die ihren Ursprung in unterschiedlichen Primärtumoren finden (Lungenkrebs, Brustkrebs, Hautkrebs etc.).
Zudem werden auch nicht tumoröse Krankheitsbilder im Bereich des Nervensystems, wie zum Beispiel Arteriovenöse Malformationen (AVM) oder die Trigeminusneuralgie mittels Strahlentherapie behandelt, die ebenfalls im Rahmen dieser Arbeitsgruppe erforscht werden.
Die Strahlentherapie kommt bei der Therapie der o.g. Krankheitsbilder häufig im Rahmen eines multimodalen Therapiekonzeptes als ein essentieller Pfeiler der onkologischen Therapie neben den weiteren Pfeilern der onkologischen Systemtherapie (Chemotherapie, Immuntherapie, zielgerichtete Therapie etc.) und der chirurgischen Therapie zur Anwendung.
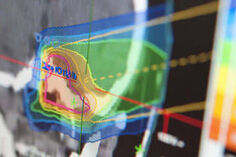
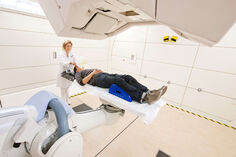
Zur Strahlentherapie dieser Krankheitsbilder stehen an der Klinik für Radioonkologie und Strahlentherapie des Universitätsklinikums Heidelberg zudem eine Vielzahl strahlentherapeutischer Techniken zur Verfügung. Neben den klassischen Linearbeschleunigern die eine 3D-Konformale (3D-CRT) oder Intensitätsmodulierte Radiotherapie (IMRT) durchführen können, bieten wir die Option unterschiedlicher stereotaktischer Radiotherapien an (z.B. mittels Cyberknife). Auch die Partikeltherapie mittels Protonen, Kohlenstoffionen und Heliumionen (am Heidelberger Ionenstrahlen-Therapiezentrum, HIT) kann eine Therapieoption bei bestimmten Tumoren oder onkologischen Situationen darstellen. Zudem besteht auch die Möglichkeit einer intraoperativen Radiotherapie (IORT) und Brachytherapie.
Ziel ist es, die (radioonkologische) Therapie nicht nur stetig weiterzuentwickeln und zu verbessern, sondern auch personalisierte Therapieansätze, angepasst an die individuellen Tumorcharakteristika sowie Bedürfnisse der PatientInnen, zu etablieren.
In enger Kooperation mit den Abteilungen Neuroonkologie, Neuropathologie, Neuroradiologie und Neurochirurgie werden eine Vielzahl moderner und innovativer Studienkonzepte zur Behandlung von primären und sekundären Tumoren des Nervensystems durchgeführt.
_______________
The working group Neuro-Radiation Oncology focusses on investigation of radiotherapeutic procedures and therapeutic approaches in the treatment of primary and secondary tumors of the nervous system. This involves a wide range of tumor entities:
These include not only primary brain tumors such as gliomas and glioblastomas (and many others), but also benign and malignant tumors of the meninges (meningiomas) and cranial nerves/spinal nerves (neurinomas), as well as secondary brain tumors such as brain metastases, which find their origin in various tumors (lung cancer, breast cancer, skin cancer, etc.).
In addition, non-tumorous clinical entities of the nervous system, such as arteriovenous malformations (AVM) or trigeminal neuralgia, are also treated by means of radiation therapy, which are also being researched within the framework of this working group.
Radiation therapy is frequently used in the treatment of the above-mentioned diseases as part of a multimodal therapy concept. This means as an essential pillar of oncological therapy besides the other pillars of oncological systemical treatment (chemotherapy, immunotherapy, targeted therapy etc.) and surgical therapy.
A wide range of radiotherapeutic techniques are also available at the Heidelberg Radiation Oncology Department of the Heidelberg University Hospital for the radiotherapy of these clinical pictures. In addition to the classic linear accelerators that can perform 3D conformal (3D-CRT) or intensity modulated radiotherapy (IMRT), we offer the option of various stereotactic radiotherapies (e.g. using Cyberknife), but also particle therapy using protons, carbon ions and also in an experimental settinghelium ions (at the Heidelberg Ion Beam Therapy Centre, HIT) can represent a therapy option for certain tumors or oncological situations. In addition, there is also the possibility of intraoperative radiotherapy (IORT).
The aim is not only to continuously develop and improve (radiooncological) therapy, but also to establish personalized therapy approaches, adapted to the individual tumor characteristics and needs of the patients.
In close cooperation with the departments of Neurooncology, Neuropathology, Neuroradiology and Neurosurgery, a variety of modern and innovative study concepts for the treatment of primary and secondary tumors of the nervous system are carried out.
Aktuelle Ausschreibungen
Medizinische Doktoranden und wissenschaftliche Hilfskräfte:
Interessieren Sie sich für unsere Arbeit und möchten sich aktiv an unserer Forschung beteiligen? Es besteht die Möglichkeit als wissenschaftliche Hilfskraft und/oder medizinische Doktoranden in unserer Arbeitsgruppe mitzuarbeiten. Wir führen keine aktualisierte Themenliste, besprechen aber sehr gerne gemeinsam mögliche Projekte. Für Fragen oder Bewerbungen kontaktieren Sie uns bitte via E-Mail.
Weitere Informationen: Medizinische Doktorarbeit: Universitätsklinikum Heidelberg (uni-heidelberg.de)
Bitte fügen Sie Ihrer Bewerbung folgende Unterlagen bei:
- Kurzes Motivationsschreiben
- Falls vorhanden: Beschreibung des Projektvorhabens
- Tabellarischer Lebenslauf
Ansprechpartnerin: Prof. Dr. Laila König

Ärztliche Mitarbeiter-/innen
Prof. Dr. med. Laila König
(Mutterschutz)
Schwerpunkt
Forschungsgruppenleiterin mit Schwerpunkt Neuro-Radioonkogie, Stereotaktische Radiotherapie/Radiochirurgie, Partikeltherapie, Intraoperative Strahlentherapie (IORT), Lymphome, Ganzkörperbestrahlungen (TBI)
PD Dr. med. Tanja Eichkorn
Schwerpunkt
Stellvertretende Forschungsgruppenleiterin mit Schwerpunkt Neuro-Radioonkogie, Stereotaktische Radiotherapie/Radiochirurgie, Partikeltherapie, Intraoperative Strahlentherapie (IORT), Gliome, Hirnmetastasen, Radiogene Schrankenstörungen/Radionekrosen
Dr. med. Angela Paul
Schwerpunkt
AVM, Stereotaktische Radiotherapie/Radiochirurgie, Cyberknife, Partikeltherapie, Vestibularisschwannome, Meningeome, Gliome und Hirnmetastasen
Dr. med. Maximilian Deng
Schwerpunkt
Meningeome, Genomisch-stratifizierte Radiotherapie in Hirntumoren, pädiatrische Radioonkologie
Dr. med. Lucas Mose
Schwerpunkt
Stereotaktische Radiotherapie/Radiochirurgie, Zerebrale Metastasen, Gliome, Urogenitale RadioOnkologie
Dr. med. Jannik Walter
Schwerpunkt
Hyperthermie, Strahlenimmunbiologie, Immuntherapie, Vestibularisschwannome
Lars Wessel
Schwerpunkt
Neuro-/Gynäko Radioonkologie, KI-Modelle in radioonkologischer Diagnostik, Stereotaktische Radiotherapie/Radiochirurgie, Gliome, Radionekrose, Partikeltherapie
Dr. med. Ricarda Maria Wickert
Schwerpunkt
Posttherapeutische radiogene Veränderungen, Meningeome, Partikeltherapie, pädiatrischen Radioonkologie
Dr. med. Ricarda Maria Wickert
Schwerpunkt
Posttherapeutische radiogene Veränderungen, Meningeome, Partikeltherapie, pädiatrischen Radioonkologie
Doktorand-/innen / offene Doktorarbeiten
- Günes Mustafa Anil
Thema: Genomisch‑stratifizierte Auswertung von Meningeompatienten nach Radiotherapie. Supervision: Dr. med. Maximilian Deng - Laura Hahnemann
Thema: Onkologische Ergebnisse und prognostische Faktoren der stereotaktischen Radiotherapie von Hirnmetastasen in Kombination mit Systemtherapien. Supervision: Prof. Dr. Laila König - Sebastian Hüske
Thema: Akut‑ und Langzeittoxizität, Therapieerfolg sowie Sekundärmalignomrate bei der Ganzkörperbestrahlung im Rahmen der Konditionierungstherapie vor Stammzelltransplantationen. Supervision: Prof. Dr. Laila König - Sophie Rauh
Thema: Präzisionsbestrahlung bei Meningeompatienten. Supervision: Dr. med. Maximilian Deng - Lisa-Marie Seidel
Thema: Einfluss molekularer Marker auf das Rezidivmuster von Meningeomen nach Radiotherapie. Supervision: Dr. med. Maximilian Deng - Angelika Reidel
Thema: Zwischenauswertung der multizentrischen Registerstudie zur Protonen-Radiotherapie bei mediastinalen Lymphomen. Supervision: Prof. Dr. Laila König - Yuliia Cherniienko
Thema: Photonenradiotherapie von Gliomen WHO Grad 1-3: Effektivität, Toxizität, Langzeitüberleben, Vergleich zur Protonenbestrahlung. Supervision: PD Dr. med. Tanja Eichkorn - Hin Lau
Supervision: Prof. Dr. Laila König - Katharina Westerhoff
Thema: Longitudinale MRT-basierte Differenzierung zwischen Tumorrezidiven und radiogenen Veränderungen bei intraaxialen zerebralen Raumforderungen mit Hilfe eines Deep-Learning-Algorithmus. Supervision: Lars Wessel - Annabella Schiele
Thema: : Validierung prognostischer Scores für Patient*innen mit multiplen Hirnmetastasen und wiederholter stereotaktischer Radiochirurgie. Supervision: Prof. Dr. med. Rami El Shafie (Göttingen)/Prof. Dr. Dr. Jürgen Debus
Kooperationspartner-/innen
- Klinik für Neurologie, Sektion Neuroonkologie – UK Heidelberg (Uni-Prof. Dr. med. Wolfgang Wick)
Ansprechpartner: Prof. Dr. med. Antje Wick, PD Dr. med. Tobias Kessler
- Neurochirurgische Klinik – UK Heidelberg (Univ.-Prof. Dr. med. Sandro Krieg, MBA)
Ansprechpartner: PD Dr. med. Sebastian Ille, PD Dr. med. Bogdana Suchorska
- Klinik für Neuroradiologie – UK Heidelberg (Uni.-Prof. Dr. med. Martin Bendszus)
Ansprechpartner: PD Dr. med. Katharina Schregel
- Forschungsgruppe Psychoonkologie – UKE Hamburg
Ansprechpartnerin: Dr. Mareike Rutenkröger
- Klinische Kooperationseinheit Translationale Radioonkologie – DKFZ
Ansprechpartner: Prof. Dr. Dr. Amir Abdollahi
- Klinische Kooperationseinheit Molekulare Radioonkologie - DKFZ
Ansprechpartner: Prof. Dr. Peter Huber
- Abteilung Medizinische Bildverarbeitung – DKFZ
Ansprechpartner: Prof. Dr. Klaus Maier‑Hein
- Abteilung Intelligente Medizinische Systeme – DKFZ
Ansprechpartnerin: Prof. Dr. Lena Maier‑Hein
- AG Stereotaktische und räumlich fraktionierte Radiotherapie
Ansprechpartner: Dr. Sebastian Regnery
- Medizinische Informatik in der Radioonkologie (MIRO) - UK Heidelberg
Ansprechpartner: Andreas Kudak, Matthias Dostal
- Neurochirurgie UK Heidelberg
Ansprechpartner: PD Dr. Maximilian Scheer, Prof. Dr. Moritz Scherer
- Neuropathologie UK Heidelberg
Ansprechpartner: Prof. Dr. Dr. Felix Sahm
Forschungsschwerpunkte/Aktuelle Projekte
Primäre Hirntumore
- Gliome und Glioblastome Gliome sind primäre Hirntumoren, die aus Stützzellen des zentralen Nervensystems (Gliazellen) hervorgehen. Man unterscheidet niedriggradige (WHO Grad 1-2) von hochgradigen Gliomen (WHO Grad 3-4) anhand ihres Wachstumsverhaltens und ihrer Prognose. Unsere Arbeitsgruppe arbeitet an unterschiedlichen Projekten um die Therapie von Gliomen zu verbessern:
Individualisierte Protonentherapie bei niedriggradigen Gliomen
Die Behandlung von Patienten mit gutartigen Hirntumoren und niedriggradigen Gliomen erfordert besonders schonende Ansätze. Die Protonentherapie ermöglicht dank ihres steilen Dosisgradienten eine präzisere Bestrahlung mit möglicher Reduktion langfristiger Nebenwirkungen. Ziel aktueller Forschungsprojekte ist es, insbesondere radiogene Schädigungen der Blut-Hirn-Schranke besser zu verstehen und zu vermeiden.
Protonentherapie beim Glioblastom – GRIPS-Studie
Bei aggressiven Tumoren wie dem Glioblastom untersucht die GRIPS-Studie, ob eine Protonentherapie gegenüber der etablierten photonbasierten Intensitätsmodulierten Radiotherapie (IMRT) Vorteile in Bezug auf Nebenwirkungen und Therapieerfolg bietet.
- Meningeome Meningeome sind primäre Hirntumoren da sie von den Hirnhäuten (Meningen) ausgehen. Sie sind meist gutartig und wachsen langsam. Es werden drei WHO-Grade unterschieden und unsere Arbeitsgruppe beschäftig sich in verschiedenen Projekten mit:
Genomisch-stratifizierte Therapieplanung
Neue Erkenntnisse aus der molekularen Diagnostik zeigen, dass Meningeome bislang teils falsch eingestuft wurden. Die aktuelle Forschung der Arbeitsgruppe prüft, ob durch molekulargenetische Subtypen eine individuellere, präzisere Entscheidung für oder gegen eine Strahlentherapie möglich ist. Ziel ist die Entwicklung einer prospektiven Studie zur personalisierten Bestrahlungsplanung bei Meningeompatienten.
- Vestibularisschwannome (Akustikusneurinome) Vestibularisschwannome, auch Akustikusneurinome genannt, sind gutartige primäre Hirntumore die langsam wachsen und als WHO-Grad I klassifiziert sind. Ihren Ursprung haben Sie vom 8. Hirnnerven, dem Nervus vestibulocochlearis. Bedingt durch Ihre Lage können die Funktionen des Hirnnerven beeinträchtigt sein, dies äußert sich durch Hörminderung, Tinnitus, Gleichgewichtsstörungen/Schwindel oder im äußersten Fall durch Kompression benachbarter Strukturen. Unsere Arbeitsgruppe beschäftigt sich in verschiedenen Projekten damit, die Therapie des Vestibularisschwannoms zu verbessern:
Kooperationsprojekt zur Lebensqualitätsmessung bei Vestibularisschwannomen
In Zusammenarbeit mit dem Universitätsklinikum Hamburg-Eppendorf unterstützen wir die Validierung der deutschen Übersetzung des Vestibular Schwannoma Quality of Life Index (VSQOL). Wir helfen den Fragebogen klinisch zu validieren, um eine verlässliche Erfassung der krankheitsspezifischen Lebensqualität im deutschsprachigen Raum zu ermöglichen.
Registerstudie zur Strahlentherapie bei Vestibularisschwannomen
In dieser prospektiven Registerstudie werden Patient:innen mit Vestibularisschwannomen eingeschlossen. Nähere Details gerne nach Kontaktaufnahme: Jannik Walter
Sekundäre Hirntumore / Hirnmetastasen
Sekundäre Hirntumoren, auch Hirnmetastasen genannt, entstehen durch Absiedlung von Krebszellen aus Tumoren außerhalb des Gehirns, z. B. aus der Lunge, Brust oder Haut. Sie sind die häufigste Form von Hirntumoren bei Erwachsenen und treten meist im Rahmen fortgeschrittener Krebserkrankungen auf. Daher beschäftigt sich unsere Arbeitsgruppe in mehreren Projekten mit z.B. der Therapieoptimierung bei mehreren Hirnmetastasen.
Präzisionsstrahlentherapie, inkl. Stereotaxie und Partikeltherapie
Die präzise, zielgerichtete Strahlentherapie ist ein zentraler Forschungsschwerpunkt der Arbeitsgruppe Neuro-Radioonkologie. Ziel ist es, Tumoren hochwirksam zu behandeln und gleichzeitig gesundes Gewebe maximal zu schonen – insbesondere im empfindlichen Bereich des zentralen Nervensystems.
- Stereotaktische Strahlentherapie mit dem CyberKnife
- Partikeltherapie am Heidelberger Ionenstrahl-Therapiezentrum (HIT)
In Zusammenarbeit mit dem Heidelberger Ionenstrahl-Therapiezentrum (HIT) werden hochpräzise Behandlungsansätze mittels Protonen- Kohlenstoff- oder Heliumionentherapie erforscht und klinisch angewendet. Die Projekte fokussieren sich auf die Reduktion von Toxizität und die Verbesserung der lokalen Tumorkontrolle, insbesondere bei schwer therapierbaren Tumoren.
Klinische Studien
Folgende klinische Studien werden durch die wissenschaftliche Arbeitsgruppe Neuro-Radioonkologie betreut (Auswahl):
CYBERCHALLENGE
- Patient:innen mit bösartigen Tumoren in fortgeschrittenen Stadien entwickeln häufig Hirnmetastasen, die sowohl die Lebenserwartung als auch die Lebensqualität einschränken. Die Therapieoptionen bei multiplen Hirnmetastasen können unterschiedlich sein und reichen von stereotaktischer Radiochirurgie (SRS), Hippocampus-sparender Ganzhirnbestrahlung (HS-WBRT) mit simultan integriertem Boost auf große Hirnmetastasen (HS-WBRT + SIB), klassischer Ganzhirnbestrahlung (WBRT), Chemotherapie, Immuntherapie bis hin zu palliativer Best Supportive Care. Insbesondere SRS im Vergleich zur (HS-WBRT +/- SIB) bei Patienten mit ausgedehnten Hirnmetastasen (>4) ist noch unklar, welche dieser beiden hochmodernen Techniken überlegen ist, aber in dieser schwer kranken Kohorte mit begrenzter Lebenserwartung von zunehmender Bedeutung. Diese gesundheitlich geschwächten Patienten könnten besonders von einer weniger toxischen Behandlung profitieren. Es ist zu erwarten, dass unterschiedliche Patient:innen in unterschiedlichen Situationen von unterschiedlichen Therapien profitieren. Ziel dieser randomisierten prospektiven Studie ist es die individualisierte Patientenversorgung bei Hirnmetastasen weiter voranzutreiben und die Frage beantworten zu können, welche Patient:innen am meisten von welcher Therapie profitieren.
GRIPS-STUDIE
- In dieser multizentrischen, randomisierten Phase-III-Studie wird die Strahlentherapie bei Glioblastom-Patient:innen mit intensitätsmodulierter Radiotherapie (IMRT) gegenüber Protonentherapie verglichen. Ziel ist die Evaluation von Wirksamkeit und Verträglichkeit beider Verfahren.
GLIOCAVE-STUDIE
- In dieser randomisierten Phase-II-Studie wird untersucht, ob eine adjuvante fraktionierte stereotaktische Strahlentherapie der Resektionshöhle bei rezidiviertem Glioblastom das Therapieergebnis verbessern kann.
REGISTERSTUDIE Vestibularisschwannome
- In dieser prospektiven Registerstudie werden Patient:innen mit Vestibularisschwannomen eingeschlossen. Nähere Details gerne nach Kontaktaufnahme: Jannik Walter
MOLI-STUDIE
- In dieser explorativen prospektiven Biomarker-Studie werden extrazelluläre Vesikel als „Liquid Biopsy“-Marker bei Meningiom-Patient:innen nach der Radiotherapie untersucht. Es soll getestet ob die Anzahl der frei-zirkulierenden extrazellulären Vesikel mit dem bildgebenden Therapieansprechen korreliert.
Kooperationspartner
LITERATUR / PUBLIKATIONEN
Link zu PubMed Prof. Dr. med. Laila König
2025
- Krämer A, Hahnemann L, Schunn F, Grott CA, Thomas M, Christopoulos P, Lischalk JW, Hörner-Rieber J, Hoegen-Saßmannshausen P, Eichkorn T, Deng MY, Meixner E, Lang K, Paul A, Weykamp F, Debus J and König L. Fractionated stereotactic radiotherapy of brainstem metastases - Clinical outcome and prognostic factors. Clin Transl Radiat Oncol (2025) 50: 100893. doi.org/10.1016/j.ctro.2024.100893
- Regnery S, Katsigiannopulos E, Lau H, Hoegen-Saßmannshausen P, Weykamp F, Renkamp CK, Rippke C, Schlüter F, Albert S, Meis J, Kirchner M, Balzer A, Andratschke N, Guckenberger M, Debus J, Klüter S and Hörner-Rieber J. How to protect the proximal bronchial tree during stereotactic radiotherapy of ultracentral lung tumors: Lessons from MR-guided treatment. Clin Transl Radiat Oncol (2025) 51: 100899. doi.org/10.1016/j.ctro.2024.100899
2024
- Alhalabi OT, Dao Trong P, Kaes M, Jakobs M, Kessler T, Oehler H, König L, Eichkorn T, Sahm F, Debus J, von Deimling A, Wick W, Wick A, Krieg SM, Unterberg AW and Jungk C. Repeat surgery of recurrent glioma for molecularly informed treatment in the age of precision oncology: A risk-benefit analysis. J Neurooncol (2024) 167(2): 245-255. https://doi.org/10.1007/s11060-024-04595-5
- Bauer L, Paul A, Regnery S, Deng MY, Ellerbrock M, Mielke T, Harrabi SB, Seidensaal K, Held T, Herfarth K, Debus J, Hassel JC and Uzun-Lang K. Bimodal intensity-modulated radiotherapy in combination with carbon ion therapy (C12) of mucosal melanomas - data of the last decade from Heidelberg University Hospital. Front Oncol (2024) 14: 1437412. https://doi.org/10.3389/fonc.2024.1437412
- Besuglow J, Tessonnier T, Mein S, Eichkorn T, Haberer T, Herfarth K, Abdollahi A, Debus J and Mairani A. Understanding Relative Biological Effectiveness and Clinical Outcome of Prostate Cancer Therapy Using Particle Irradiation: Analysis of Tumor Control Probability With the Modified Microdosimetric Kinetic Model. Int J Radiat Oncol Biol Phys (2024) 119(5): 1545-1556. https://doi.org/10.1016/j.ijrobp.2024.02.025
- Beyer C, Paul KM, Dorsch S, Echner G, Dinkel F, Welzel T, Seidensaal K, Hörner-Rieber J, Jäkel O, Debus J and Klüter S. Compliance of volunteers in a fully-enclosed patient rotation system for MR-guided radiation therapy: a prospective study. Radiat Oncol (2024) 19(1): 71. https://doi.org/10.1186/s13014-024-02461-2
- Bonaccorsi SG, Tessonnier T, Hoeltgen L, Meixner E, Harrabi S, Hörner-Rieber J, Haberer T, Abdollahi A, Debus J and Mairani A. Exploring Helium Ions' Potential for Post-Mastectomy Left-Sided Breast Cancer Radiotherapy. Cancers (Basel) (2024) 16(2). https://doi.org/10.3390/cancers16020410
- Buchele C, Renkamp CK, Regnery S, Behnisch R, Rippke C, Schlüter F, Hoegen-Saßmannshausen P, Debus J, Hörner-Rieber J, Alber M and Klüter S. Intrafraction organ movement in adaptive MR-guided radiotherapy of abdominal lesions - dosimetric impact and how to detect its extent in advance. Radiat Oncol (2024) 19(1): 80. https://doi.org/10.1186/s13014-024-02466-x
- Deng MY, da Silva AS, Göller PC, König L, Schäfer H, Maire C, Lentz-Hommertgen A, Held T, Regnery S, Eichkorn T, Stritzke F, Bauer L, Schnell D, Herfarth K, von Deimling A, Krieg S, Wick A, Wick W, Grosu A, Debus J, Sahm F and Ricklefs F. Plasma extracellular vesicles in meningioma patients following radiotherapy as liquid biopsy- a prospective explorative biomarker study (ARO 2023-05/AG-NRO-07). BMC Cancer (2024) 24(1): 449. https://doi.org/10.1186/s12885-024-12170-4
- Deng MY, Maas SLN, Hinz F, Karger CP, Sievers P, Eichkorn T, Meixner E, Hoegen-Sassmannshausen P, Hörner-Rieber J, Lischalk JW, Seidensaal K, Bernhardt D, Jungk C, Unterberg A, Wick A, Wick W, von Deimling A, Sahm F, Combs S, Herfarth K, Debus J and König L. Efficacy and toxicity of bimodal radiotherapy in WHO grade 2 meningiomas following subtotal resection with carbon ion boost: Prospective phase 2 MARCIE trial. Neuro Oncol (2024) 26(4): 701-712. https://doi.org/10.1093/neuonc/noad244
- Deng MY, Rauh S, Anil G, Lischalk JW, Hahnemann L, Eichkorn T, Hörner-Rieber J, Paul A, Sandrini E, Hoegen-Sassmannshausen P, Held T, Regnery S, Bauer L, Sahm F, von Deimling A, Wick A, Wick W, Jungk C, Krieg SM, Herfarth K, Debus J and König L. Analysis of safety and efficacy of proton radiotherapy for optic nerve sheath meningioma. Neuro-oncology advances (2024) 6(1): vdae160. https://doi.org/10.1093/noajnl/vdae160
- Deng MY, Sahm F, Debus J and König L. [A 34-gene expression biomarker to predict oncologic outcome and treatment response after radiotherapy in meningioma]. Strahlenther Onkol (2024) 200(10): 916-918. https://doi.org/10.1007/s00066-024-02268-w
- Eichkorn T, Lischalk JW, Schwarz R, Bauer L, Deng M, Regnery S, Jungk C, Hörner-Rieber J, Herfarth K, König L and Debus J. Radiation-Induced Cerebral Contrast Enhancements Strongly Share Ischemic Stroke Risk Factors. Int J Radiat Oncol Biol Phys (2024) 118(5): 1192-1205. https://doi.org/10.1016/j.ijrobp.2023.12.044
- Elsayad K, Guenova E, Assaf C, Nicolay JP, Trautinger F, Stadler R, Waldstein C, Boterberg T, Meijnders P, Kirova Y, Dobos G, Duque-Santana V, Riggenbach E, Elsheshtawy W, Niezink A, Papadavid E, Scarisbrick J, Vermeer M, Neelis KJ, Bagot M, Battistella M, Quaglino P, Knobler R, Kempf W, Maklad A, Adeberg S, Kouloulias V, Simontacchi G, Corradini S, König L, Eich HT, Cowan R and Correia D. Radiotherapy in cutaneous lymphomas: Recommendations from the EORTC cutaneous lymphoma tumour group. Eur J Cancer (2024) 212: 115064. https://doi.org/10.1016/j.ejca.2024.115064
- Fink CA, Buchele C, Baumann L, Liermann J, Hoegen P, Ristau J, Regnery S, Sandrini E, König L, Rippke C, Bonekamp D, Schlemmer HP, Debus J, Koerber SA, Klüter S and Hörner-Rieber J. Dosimetric benefit of online treatment plan adaptation in stereotactic ultrahypofractionated MR-guided radiotherapy for localized prostate cancer. Front Oncol (2024) 14: 1308406. https://doi.org/10.3389/fonc.2024.1308406
- Fink CA, Ristau J, Buchele C, Klüter S, Liermann J, Hoegen-Saßmannshausen P, Sandrini E, Lentz-Hommertgen A, Baumann L, Andratschke N, Baumgartl M, Li M, Reiner M, Corradini S, Hörner-Rieber J, Bonekamp D, Schlemmer HP, Belka C, Guckenberger M, Debus J and Koerber SA. Stereotactic ultrahypofractionated MR-guided radiotherapy for localized prostate cancer - Acute toxicity and patient-reported outcomes in the prospective, multicenter SMILE phase II trial. Clin Transl Radiat Oncol (2024) 46: 100771. https://doi.org/10.1016/j.ctro.2024.100771
- Hahnemann L, Krämer A, Fink C, Jungk C, Thomas M, Christopoulos P, Lischalk JW, Meis J, Hörner-Rieber J, Eichkorn T, Deng M, Lang K, Paul A, Meixner E, Weykamp F, Debus J and König L. Fractionated stereotactic radiotherapy of intracranial postoperative cavities after resection of brain metastases - Clinical outcome and prognostic factors. Clin Transl Radiat Oncol (2024) 46: 100782. https://doi.org/10.1016/j.ctro.2024.100782
- Hoegen-Saßmannshausen P, Jessen I, Buchele C, Schlüter F, Rippke C, Renkamp CK, Weykamp F, Regnery S, Liermann J, Meixner E, Hoeltgen L, Eichkorn T, König L, Debus J, Klüter S and Hörner-Rieber J. Clinical Outcomes of Online Adaptive Magnetic Resonance-Guided Stereotactic Body Radiotherapy of Adrenal Metastases from a Single Institution. Cancers (Basel) (2024) 16(12). https://doi.org/10.3390/cancers16122273
- Hoegen-Saßmannshausen P, Naumann P, Hoffmeister-Wittmann P, Ben Harrabi S, Seidensaal K, Weykamp F, Mielke T, Ellerbrock M, Habermehl D, Springfeld C, Dill MT, Longerich T, Schirmacher P, Mehrabi A, Chang DH, Hörner-Rieber J, Jäkel O, Haberer T, Combs SE, Debus J, Herfarth K and Liermann J. Carbon ion radiotherapy of hepatocellular carcinoma provides excellent local control: The prospective phase I PROMETHEUS trial. JHEP reports : innovation in hepatology (2024) 6(6): 101063. https://doi.org/10.1016/j.jhepr.2024.101063
- Hoeltgen L, Meixner E, Hoegen-Saßmannshausen P, Kim JY, Deng M, Seidensaal K, Held T, Herfarth K, Haberer T, Debus J, Mairani A, Harrabi S and Tessonnier T. Helium Ion Therapy for Advanced Juvenile Nasopharyngeal Angiofibroma. Cancers (Basel) (2024) 16(11). https://doi.org/10.3390/cancers16111993
- Kim JY, Tawk B, Knoll M, Hoegen-Saßmannshausen P, Liermann J, Huber PE, Lifferth M, Lang C, Häring P, Gnirs R, Jäkel O, Schlemmer HP, Debus J, Hörner-Rieber J and Weykamp F. Clinical Workflow of Cone Beam Computer Tomography-Based Daily Online Adaptive Radiotherapy with Offline Magnetic Resonance Guidance: The Modular Adaptive Radiotherapy System (MARS). Cancers (Basel) (2024) 16(6). https://doi.org/10.3390/cancers16061210
- Meixner E, Glogauer B, Klüter S, Wagner F, Neugebauer D, Hoeltgen L, Dinges LA, Harrabi S, Liermann J, Vinsensia M, Weykamp F, Hoegen-Saßmannshausen P, Debus J and Hörner-Rieber J. Validation of different automated segmentation models for target volume contouring in postoperative radiotherapy for breast cancer and regional nodal irradiation. Clin Transl Radiat Oncol (2024) 49: 100855. https://doi.org/10.1016/j.ctro.2024.100855
- Meixner E, Hoeltgen L, Dinges LA, Harrabi S, Seidensaal K, Weykamp F, Hoegen-Sassmanshausen P, Vinsensia M, König L, Deng M, Debus J and Hörner-Rieber J. Efficacy of palliative hemostatic radiotherapy for tumor bleeding and pain relief in locally advanced pelvic gynecological malignancies. Strahlenther Onkol (2024). https://doi.org/10.1007/s00066-024-02319-2
- Meixner E, Wermes L, Hoeltgen L, von Diest LA, Sandrini E, Harrabi S, Seidensaal K, Hoegen-Saßmannshausen P, Vinsensia M, König L, Arians N, Debus J and Hörner-Rieber J. Hematologic Toxicity Profiles and the Impact of Hemoglobin Nadir and Transfusion on Oncologic Outcome in Definitive Radiochemotherapy for Cervical Cancer. Cancers (Basel) (2024) 16(23). https://doi.org/10.3390/cancers16233986
- Paul K, Dorsch S, Elter A, Beyer C, Naumann J, Hansmann T, Feldmeier E, Haberer T, Karger CP, Debus J and Klüter S. Online MR-guided proton and ion beam radiotherapy: investigation of image quality. Phys Med Biol (2024) 69(18). https://doi.org/10.1088/1361-6560/ad7453
- Roohani S, Mirwald M, Ehret F, Fink C, König L, Striefler JK, Jacob NS, Popp I, Steffel J, Handtke J, Claßen NM, Rotermund T, Zips D, Vajkoczy P, Schüller U, Spałek MJ and Kaul D. Gliosarcoma: A Multi-Institutional Analysis on Clinical Outcomes and Prognostic Factors. Cancer Med (2024) 13(22): e70347. https://doi.org/10.1002/cam4.70347
- Ton M, Deng M, Meixner E, Eichkorn T, Krämer A, Seidensaal K, Hörner-Rieber J, Lischalk J, Herfarth K, Debus J and König L. Efficacy and toxicity of photon, proton, and carbon ion radiotherapy in the treatment of intracranial solitary fibrous tumor/hemangiopericytoma. Radiat Oncol (2024) 19(1): 42. https://doi.org/10.1186/s13014-024-02434-5
- Vinsensia M, Schaub R, Meixner E, Hoegen P, Arians N, Forster T, Hoeltgen L, Köhler C, Uzun-Lang K, Batista V, König L, Zivanovic O, Hennigs A, Golatta M, Heil J, Debus J and Hörner-Rieber J. Incidence and Risk Assessment of Capsular Contracture in Breast Cancer Patients following Post-Mastectomy Radiotherapy and Implant-Based Reconstruction. Cancers (Basel) (2024) 16(2). https://doi.org/10.3390/cancers16020265
- Walter A, Hoegen-Saßmannshausen P, Stanic G, Rodrigues JP, Adeberg S, Jäkel O, Frank M and Giske K. Segmentation of 71 Anatomical Structures Necessary for the Evaluation of Guideline-Conforming Clinical Target Volumes in Head and Neck Cancers. Cancers (Basel) (2024) 16(2). https://doi.org/10.3390/cancers16020415
- Wark A, Gupta A, Meixner E, König L, Hörner-Rieber J, Forster T, Lang K, Ellerbrock M, Herfarth K, Debus J and Arians N. Bone Marrow Sparing by Intensity Modulated Proton Beam Therapy in Postoperative Irradiation of Gynecologic Malignancies. Technol Cancer Res Treat (2024) 23: 15330338241252622. https://doi.org/10.1177/15330338241252622
- Weykamp F, Meixner E, Arians N, Hoegen-Saßmannshausen P, Kim JY, Tawk B, Knoll M, Huber P, König L, Sander A, Mokry T, Meinzer C, Schlemmer HP, Jäkel O, Debus J and Hörner-Rieber J. Daily AI-Based Treatment Adaptation under Weekly Offline MR Guidance in Chemoradiotherapy for Cervical Cancer 1: The AIM-C1 Trial. Journal of clinical medicine (2024) 13(4). https://doi.org/10.3390/jcm13040957
- Yawson AK, Walter A, Wolf N, Klüter S, Hoegen P, Adeberg S, Debus J, Frank M, Jäkel O and Giske K. Essential parameters needed for a U-Net-based segmentation of individual bones on planning CT images in the head and neck region using limited datasets for radiotherapy application. Phys Med Biol (2024) 69(3). https://doi.org/10.1088/1361-6560/ad1996