-
Molecular Neuroimmunology Group | AG Molekulare Neuroimmunologie
- About us | Über uns
- DONATIONS | SPENDENKONTO
- Staff | Mitarbeiter
- Clincial studies | Klinische Studien
- Multiple sclerosis | Multiple Sklerose
- MOG antibody-associated disease (MOGAD) | MOG-Enzephalomyelitis (MOG-EM)
- Neuromyelitis optica spectrum disorders (NMOSD) / Neuromyelitis-optica-Spektrum-Erkrankungen
- Autoimmune encephalitis and paraneoplastic neurological syndromes / Autoimmunenzephalitiden und paraneoplastische neurologische Syndrome
- COVID-19/SARS-CoV-2 and Post-/Long-COVID | COVID-19/SARS-CoV-2 und Post-/Long-COVID
- Baló's concentric sclerosis (BCS) / Konzentrische Sklerose Baló
- Schilder's myelinoclastic diffuse sclerosis (MDS) | Myelinoklastische diffuse Sklerose (Morbus Schilder)
- History of neuroscience | Geschichte der Neurowissenschaften
- MMN and CIDP | MMN und CIDP
- Neoplasms | Neoplasien
- Neuroinflammation & Degeneration
- DFG Forschergruppe 2289
- Neuroinfectiology
Arbeitsgruppe Neuroinfektiologie und Neurotransmission
Arbeitsgruppenleiter

Doktorarbeiten
Die Arbeitsgruppe vergibt ab Mitte 2012 wieder Doktorarbeiten. Informationen und Kontakt über Herrn Dr. Lenhard.
Forschungsschwerpunkte
- Pathomechanismen und Molekularbiologie viraler Meningoenzephalitiden
- Regulation der Bluthirnschrankenfunktion durch Pathogene und Mechanismen ihrer Neurotransmission
- Entwicklung onkolytischer Herpesviren
Die Forschungsgruppe interessiert sich für die Pathomechanismen von Infektionen des Gehirns. Im Vordergrund stehen dabei virale Meningoenzephalitiden, mit einem Schwerpunkt auf der Herpes-Simplex-Virus Enzephalitis (HSVE) und Flaviviraler Enzephalitiden (bspw. Tick-Borne Encephalitis, TBE; FSME). Methodisch arbeiten wir sowohl mit Tiermodellen (murines HSVE-Modell) wie auch mit unterschiedlichen Zellkulturmodellen einschließlich einem breiten Spektrum zellbiologischer und molekularbiologischer Methoden. Forschungsergebnisse aus den zurückliegenden 10 Jahren haben in eine Therapiestudie zur humanen HSVE gemündet: German trial of Acyclovir and corticosteroids in Herpes-simplex-virus-encephalitis (GACHE): a multicenter, multinational, randomized, double-blind, placebo-controlled German, Austrian and Dutch trial (Current Controlled Trials ISRCTN45122933; Bmbf Grant Number 01KG0504).
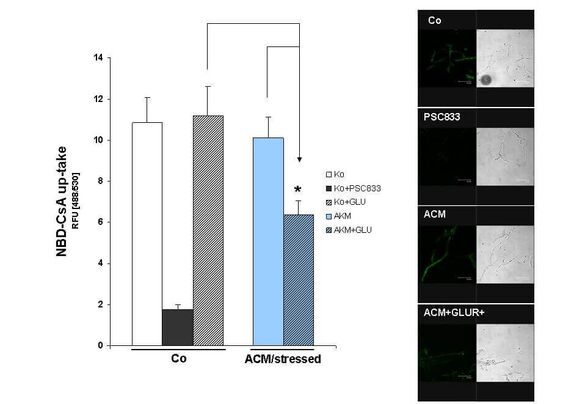
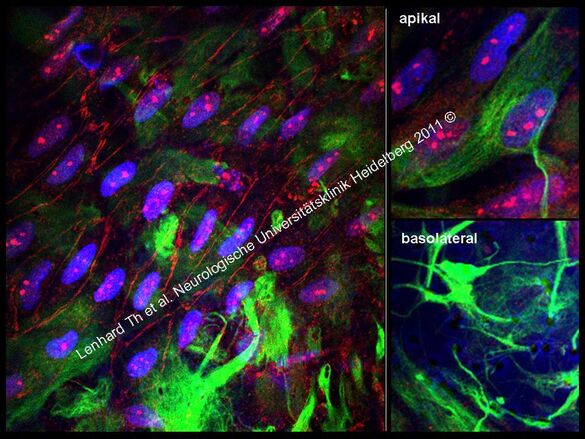
Die Arbeitsgruppe interessiert sich mit einem weiteren Forschungsschwerpunkt für die zellulären und molekularen Mechanismen mikrobieller Neurotransmission. Dazu wurde ein murines in-vitro Blut-Hirn-Schranken-Modell etabliert und weiterentwickelt. Ein permanentes humanes Modell ist in Entwicklung. Neben Grundlagen orientierten Fragen, in wieweit lösliche Faktoren aber auch Zell-Zell-Wechselwirkungen zwischen Astrozyten und der basolateralen Seite von Endothelien die Funktion der Blut-Hirn-Schranke regulieren, sind wir auch daran interessiert zu verstehen, wie eine virale Infektion die Blut-Hirn-Schrankenfunktion reguliert respektive beeinträchtigt und welche molekularen Mechanismen der Neurotransmission von Viren über das zerebrale Endothel zugrunde liegen.
Projekte
Neurotransmission von TBEV in-vitro
FSME-Viren oder auch TBEV gehören zu den Flaviviridae, einer Familie kleiner, behüllter Viren mit einem positiven RNA-Strang als Genom. Weitere Vertreter der Flaviviridae sind bspw. das Dengue-, Japan-Enzephalitis oder West-Nil-Virus. TBEV messen ca. 40-60 nm im Durchmesser und ihr 10,8 kb großes Genom kodiert für insgesamt 3 Strukturgene (pM, pE, Capsid) und für 4 weitere, regulatorische Gene. Durch den Stich von Ixodes ricinus (gemeiner Holzbock) wird TBEV in die Haut übertragen und infiziert zunächst Langerhanszellen, die das Virus in lymphoide Organe propagieren, wo eine weitere Virusreplikation stattfindet. Dies führt in ca. 30 % der so Infizierten zur Virämie (katarrhalische Phase). In einer zweiten Phase kommt es in ca. weiteren 30% der Individuen zur Neurotransmission mit Entwicklung einer Meningitis (ca. 50%), Meningoenzephalitis (ca. 40%) oder in schweren Fällen auch einer Meningoenzephaloradikulitis (<10%). Die Mechanismen, wie TBEV die Blut Hirn Schranke überwindet, sind bislang kaum aufgeklärt. Sehr wahrscheinlich kommt es dabei zunächst zu einer Infektion zerebraler Endothelien. Die Virusbindung an Wirtszellen und die virale Endozytose wird über pE vermittelt. Der wirtsständige Rezeptor ist bis heute nicht eindeutig bekannt. Mehrere Proteine, die TBEV binden können, darunter ein Nicht-Integrin-Lamininrezeptor, wurden identifiziert. TBEV muss entweder einen ubiquitären und über verschiedene Spezies (Arthropoden, Nager, Mensch) hoch konservierten Rezeptor nutzen oder an mehrere verschiedene Rezeptoren binden können. Mit Hilfe des Blut-Hirn-Schranken-Modells wollen wir Mechanismen der Neurotransmission genauer studieren und mögliche wirtsständige Rezeptoren identifizieren.
Prävalenz und Virusstammanalysen von TBEV in Ixodes ricinus in einem Endemiegebiet der TBE
Heidelberg liegt an den westlichen Hängen des Odenwaldes. Der Odenwald ist ein Endemiegebiet für TBEV und die östlich von Heidelberg gelegenen Landkreise sind Risiko- und zum Teil Hochrisikogebiete der TBE (RKI-Bulletin 18/2008). Wir beobachten seit Mitte der 90er Jahre eine Zunahme schwerer und schwerster TBE-Verläufe in den Endemiegebieten. Wir untersuchen, inwieweit diese Zunahme auf eine Prävalenzzunahme von TBEV in Ixodes ricinus zurückgeht und/oder inwieweit Virus-abhängige Faktoren eine Rolle spielen, wie beispielsweise eine Zunahme der Virulenz durch Mutationen.
Building up and establishing a molecular biological laboratory for the diagnostic routines of viral infections in Brunei: concepts for stuff qualification, quality validation, infection surveillance and scientific application
In einer Kooperation mit der Neurologischen Klinik des Krankenhaus Nordwest Frankfurt und der Universiti Brunei Darussalam (UBD) auf Borneo. Im Rahmen eines Joint-ventures zum mehrstufigen Aufbau eines Labors zur Liquordiagnostik und Diagnostik von Neuroinfektionen an der Universitätsklinik sollen mit einem gemeinsamen interdisziplinären wissenschaftlichen Projekt zusammen mit Klinikern, Virologen und unserer Arbeitsgruppe ortstypische virale Infektionen des Gehirns hinsichtlich epidemiologischer Kenndaten, ihrer klinischen Merkmale und Verläufe sowie ihres inflammatorischen Proteoms möglichst umfassend charakterisiert. Dieses Projekt wird Anfang 2012 starten. Mitte 2012 werden dazu auch Doktorarbeiten ausgeschrieben werden.
Charakterisierung von natürlichen und induzierten HSV-Mutanten
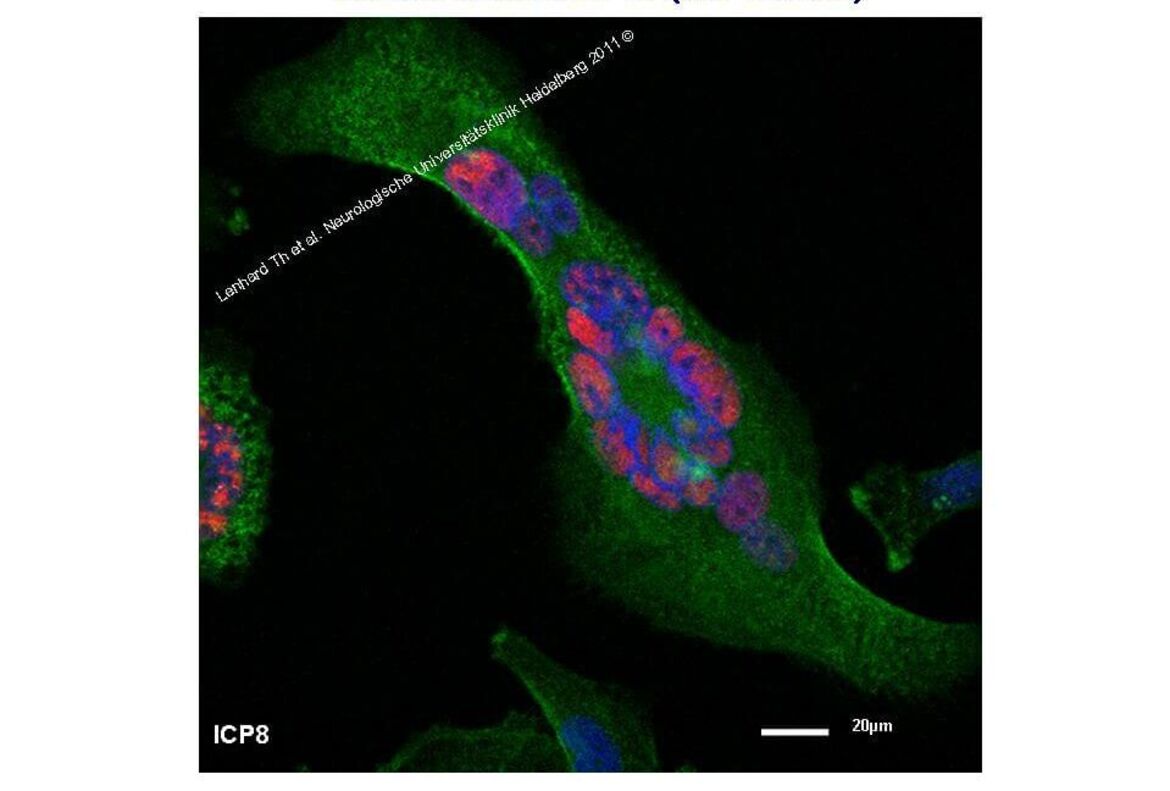
Wir verfügen über einen Fundus von Wildtyp-HSV, Wildtyp-Mutanten oder auch rekombinant erzeugte HSV. Diese zeigen in Abhängigkeit von Mutationen unterschiedlicher Gene ein zell-restriktives Infektions- und Replikationsverhalten in neuronalen Zellen - bis hin zu einem apathogenen Phänotyp. Wir sind an den molekularen Mechanismen hinter diesen Phänotypen, dabei besonders an der Wechselwirkung viraler Replikations-regulierender Gene mit wirtszellulären Genen interessiert. Im Fokus stehen hier die Entwicklung von HSV-basierten Vektoren zur transgenen Expression in neuronalen Zellen sowie onkolytischer Viren.
Kooperationen (Deutschland)
Prof. Dr. G. Fricker; Institut für Pharmazie & Biotechnologie, Abt. Pharmazeutische Technologie, INF 366, Universität Heidelberg
Fr. Dr. U. Hülsermann; Institut für Pharmazie & Biotechnologie, Universität Heidelberg (aktuelle Adresse: Spitzner GmbH, Ettlingen)
Fr. Prof. Dr. B. Wildemann; Sektion Molekulare Neuroimmunologie, OMZ, INF 350, Universitätsklinikum Heidelberg
Dr. R. Öhme; Molekularbiologie, Ref. 93, Allg. Hygiene und Infektionsschutz, Landesgesundheitsamt, Nordbahnhofstr. 135, 70191 Stuttgart
Fr. Dr. O. Bock-Hensley; Gesundheitsamt Heidelberg, Landratsamt Rhein-Neckar-Kreis, Kurfürstenanlage 38-40, 69115 Heidelberg
Dr. U. Falk; Gesundheitsamt, Michelstädter Straße 12, 64711 Erbach
Dr. R. Kehm; Abt. Biotechnologie und Sicherheit, INF 345, Universität Heidelberg
Fr. Prof. Ch. Herold-Mende; Molekularbiologisches Labor, Neurochirurgische Klinik, INF 400, UniversitätsKlinikum Heidelberg
Dr. K. Geletneky; Neurochirurgische Klinik, INF 400, UniversitätsKlinikum Heidelberg
[letzte Änderung 12.12.2011/PR]
-
Molecular Neuroimmunology Group | AG Molekulare Neuroimmunologie
- About us | Über uns
- DONATIONS | SPENDENKONTO
- Staff | Mitarbeiter
- Clincial studies | Klinische Studien
- Multiple sclerosis | Multiple Sklerose
- MOG antibody-associated disease (MOGAD) | MOG-Enzephalomyelitis (MOG-EM)
- Neuromyelitis optica spectrum disorders (NMOSD) / Neuromyelitis-optica-Spektrum-Erkrankungen
- Autoimmune encephalitis and paraneoplastic neurological syndromes / Autoimmunenzephalitiden und paraneoplastische neurologische Syndrome
- COVID-19/SARS-CoV-2 and Post-/Long-COVID | COVID-19/SARS-CoV-2 und Post-/Long-COVID
- Baló's concentric sclerosis (BCS) / Konzentrische Sklerose Baló
- Schilder's myelinoclastic diffuse sclerosis (MDS) | Myelinoklastische diffuse Sklerose (Morbus Schilder)
- History of neuroscience | Geschichte der Neurowissenschaften
- MMN and CIDP | MMN und CIDP
- Neoplasms | Neoplasien
- Neuroinflammation & Degeneration
- DFG Forschergruppe 2289
- Neuroinfectiology






